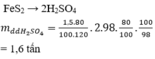2. cho 60 ký quặng pyrít sắt . hãy tính lượng dung dịch axit sunfuric 96% thu được từ quặng trên . nếu H% phản ứng đạt 85% so với lý thuyết

Những câu hỏi liên quan
1. Cho 1,12 lít khí SO2 (đktc) lội qua dung dịch Ca(OH)2 dư thu được một kết tủa. Tính khối lượng kết tủa này biết hiệu suất phản ứng là 80%?
2. Tính khối lượng axit sunfuric 96% thu được từ 60Kg quặng Pirit sắt nếu hiệu suất quá trình là 85%?
1.do hiệu suất nên nSO2=0,04(mol)
nCaSO3=0,04(mol)
\(\Rightarrow\) mCaSO3=4,8(mol)
Đúng 0
Bình luận (0)
Tính lượng axit H2SO4 thu đc từ 60 kg quặng pirit nếu PỨ là 85% so vs lý thuyết
\(n_{FeS_2}=\dfrac{60}{120}\cdot85\%=0.425\left(kmol\right)\)
\(2FeS_2\rightarrow SO_2\rightarrow SO_3\rightarrow H_2SO_4\)
\(0.425...................................0.2125\)
\(m_{H_2SO_4}=0.2125\cdot98=20.825\left(kg\right)\)
Đúng 2
Bình luận (0)
Cho 60kg FeS2. Tính lượng dung dịch H2SO4 96% thu được từ quặng trên nếu hiệu suất phản ứng là 80% so với lí thuyết.
(1) 2FeS2 + \(\dfrac{11}{2}\) O2 -to\(\rightarrow\) Fe2O3 + 4SO2
(2) SO2 \(\rightarrow\) SO3 \(\rightarrow\) H2SO4
Theo (1) và (2) : n\(H_2 SO_4\) = n\(SO_2\) = 2n\(Fe S_2\) = \(\dfrac{60 000}{120}\) . 2 = 1000 (mol)
Do hiệu suất phản ứng bằng 80% so với lý thuyết nên n\(H_2 SO_4\) (thực tế) = 80% . 1000 = 800 (mol)
\(\rightarrow\) m\(H_2 SO_4\) = 800 . 98 = 78400 (g)
\(\rightarrow\) m dd \(H_2 SO_4\) = 78400 : 96% \(\approx\) 81666,67 (g) \(\approx\) 81,67(kg)
Vậy ...
Ciao_
Đúng 0
Bình luận (0)
a) Từ 60 kg quặng pirit sắt. Tính lượng H2SO4 96% thu đc từ quặng trên nếu hiệu suất là 85% so vs lý thuyết
b) Từ 80 tấn quặng pirit chứa 40% S sản xuất đc 92 tấn H2SO4.Hãy tính hiệu suất của quá trình
a) Điều chế H2SO4 từ FeS2 qua các dãy biến hóa sau:
FeS2 -> 2SO2 -> 2SO3 -> 2H2SO4
120kg....................................2x98 kg
60kg.....................................98kg
Theo lý thuyết khối lượng H2SO4 sinh ra là 98 kg, nhưng hiệu suất 85% nên thực tế chỉ thu đc:
(98 x 85 ) : 100 = 83,3 kg
Khối lượng dd H2SO4 96% thu đc là:
100 kg dd có 96 kg H2SO4
x kg dd có 83,3 kg
=> x = (83,3 . 100 ) : 96 = 86,77 kg
Đúng 0
Bình luận (1)
b) Lượng S trong 80 tấn quặng pirit
(40 . 80) : 100 = 32 tấn
Điều chế H2SO4 từ S qua dãy biến hóa sau:
S -> SO2 -> SO3 -> H2SO4
32 tấn.......................98 tấn
Nếu tính theo lý thuyết ta thu đc 98 tấn H2SO4
Vậy hiệu suất của quá trình là: (92 x 100) : 98 = 93,88 %
Đúng 0
Bình luận (0)
Bạn ơi cho mình hỏi là bạn lấy 85% ở đâu ạ
Đúng 0
Bình luận (0)
Cho m gam bột sắt vào dung dịch axit sunfuric (H2SO4) 2M. Phản ứng xong thu được 4,48 (l) khí hiđro (đktc)
a. Viết phương trình hóa học của thí nghiệm trên.
b. Tính khối lượng sắt đã tham gia phản ứng.
c. Tính thể tích của dung dịch axit sunfuric (H2SO4) cần dùng.
Xác định khối lượng axit sunfuric có thể thu được từ 16 tấn quặng có chứa 60% FeS2. Biết hiệu suất mỗi phản ứng là 95%.
A. 6,772 tấn
B. 7,448 tấn
C. 13,444 tấn
D. 14,896 tấn
Đáp án C
Quy trình sản xuất H2SO4 trong công nghiệp:

Đúng 0
Bình luận (0)
Xác định khối lượng axit sunfuric có thể thu được từ 16 tấn quặng có chứa 60% FeS2. Biết hiệu suất mỗi phản ứng là 95%.
A. 6,772 tấn
B. 7,448 tấn
C. 13,444 tấn
D. 14,896 tấn
từ 60kg quặng pirit,tính khối lượng H2SO4 thu được,hiệu suất quá trình phản ứng là 85%
tính khối lượng dd H2SO4 96% thu được.
a) Điều chế H2SO4 từ FeS2 qua các dãy biến hóa sau:
FeS2 -> 2SO2 -> 2SO3 -> 2H2SO4
120kg....................................2x98 kg
60kg.....................................98kg
Theo lý thuyết khối lượng H2SO4 sinh ra là 98 kg, nhưng hiệu suất 85% nên thực tế chỉ thu đc:
(98 x 85 ) : 100 = 83,3 kg
Khối lượng dd H2SO4 96% thu đc là:
100 kg dd có 96 kg H2SO4
Đúng 3
Bình luận (0)
Trong công nghiệp, axit sunfuric được điều chế từ quặng pirit sắt. Khối lượng dung dịch
H
2
S
O
4
98% điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80%
F
e
S
2
(hiệu suất toàn quá trình là 80%) là A. 0,80 tấn B. 1,60 tấn C. 1,25 tấn D. 2,00 tấn
Đọc tiếp
Trong công nghiệp, axit sunfuric được điều chế từ quặng pirit sắt. Khối lượng dung dịch H 2 S O 4 98% điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80% F e S 2 (hiệu suất toàn quá trình là 80%) là
A. 0,80 tấn
B. 1,60 tấn
C. 1,25 tấn
D. 2,00 tấn